Nat Cancer |这套生信代码相当完美,图真好看,单细胞免疫图谱——多发性骨髓瘤(MM)骨髓免疫微环境
- 2026-03-03 16:20:10
日常好的代码已放入免💰共享服务器中(人人皆可用):https://vip.r-py.com/
1. 核心说明文件
- README.md(说明)
2. 细胞注释字典(cell_annotation_dictionary/)
存放 MMRF 免疫图谱中 106 个独立细胞簇的注释说明文件,包含:
补充说明文档( .md/.pdf格式)说明性 RMarkdown 文件( README.rmd)
3. 原始数据处理(processing_raw_data/)
涵盖原始单细胞数据的核心预处理流程,包含子模块:
环境 RNA 去除(Ambient_RNA_removal/)
双细胞检测(Doublet_detection/)
小鼠细胞去除(Mouse_cell_removal/)
轨迹构建(Trajectory_Construction/)
验证队列标签映射(Validation_Cohort_Label_Mapping/)
细胞元数据构建脚本(construct_cell_metadata.R)
模块说明文档(README.md) 
4. 批量效应校正(batch_correction/)
批量效应校正的说明文档(README.md) 基于 harmony 算法、PC25 维度的校正脚本(harmony_PC25_github.R) 
5. 论文图表(manuscript_figures/)
存放用于生成论文图表的代码,按图表编号分文件夹(figure_1/ 至 figure_7/),包含历史版本代码(LEGACY/)及说明文档(README.md)
突破性研究构建多发性骨髓瘤骨髓免疫图谱 为精准治疗提供新靶点
近日,一项发表于《Nature Cancer》的重磅研究成功构建了多发性骨髓瘤(MM)骨髓免疫微环境的单细胞免疫图谱,通过解析近 140 万个细胞的基因表达特征,揭示了免疫功能异常与疾病进展、预后的关键关联,为优化风险分层和开发新型免疫疗法提供了重要依据。该研究由多国科研团队联合开展,对 337 名新诊断患者的骨髓样本进行了系统分析。


多发性骨髓瘤作为全球第二大血液系统恶性肿瘤,尽管治疗手段不断进步,但仍难以治愈,每年美国新增病例超 3.5 万例,死亡人数达 1.2 万。此前研究多聚焦于肿瘤细胞自身的遗传异常,而骨髓免疫微环境对疾病发生和治疗响应的影响尚未明确。随着 CAR-T 细胞等免疫疗法的获批,解析骨髓中的免疫细胞动态成为破解治疗瓶颈的关键。

研究团队通过单细胞 RNA 测序技术,对 263 名发现队列患者的 114 万余个骨髓细胞和 74 名验证队列患者的 24 万余个细胞进行了深度分析,成功绘制出包含 T 细胞、NK 细胞、B 细胞、髓系细胞等多种免疫细胞的全景图谱。结果显示,基线骨髓微环境中 T 细胞占比最高,其中 CD8+ T 细胞占 30.51%,CD4+ T 细胞占 23.39%,同时鉴定出细胞毒性 CD4+ T 细胞等罕见细胞群体。
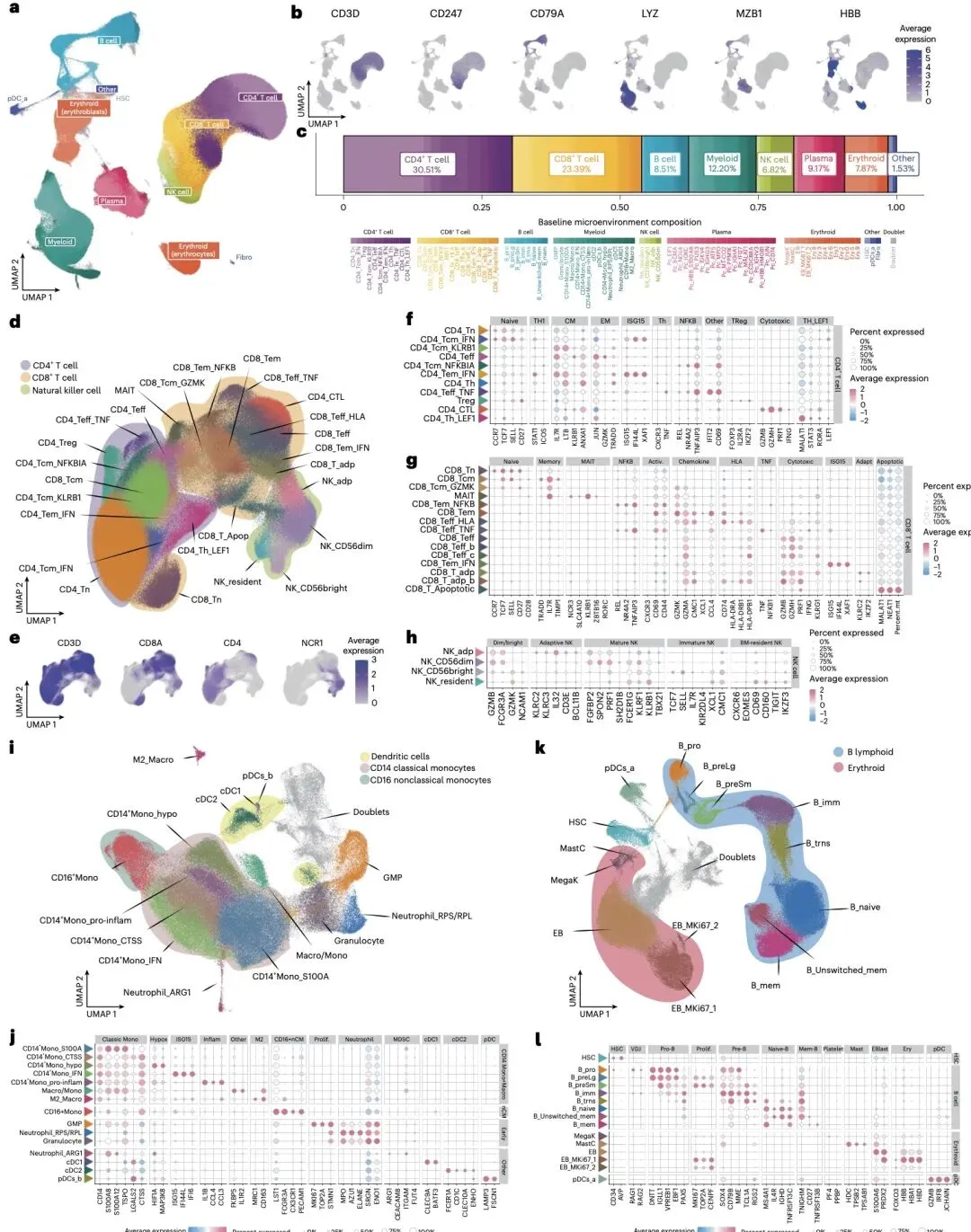
在细胞遗传学分析中,研究发现不同遗传异常对免疫细胞的影响存在显著异质性。其中 17p13 缺失患者表现出独特的 I 型干扰素信号富集特征,而 1q21 扩增和 NSD2 易位患者则出现 CD4 + 干扰素反应性记忆细胞减少。值得关注的是,高风险患者中 CD8+ HLA + 效应 T 细胞的富集与不良预后密切相关,其总体生存率显著降低。
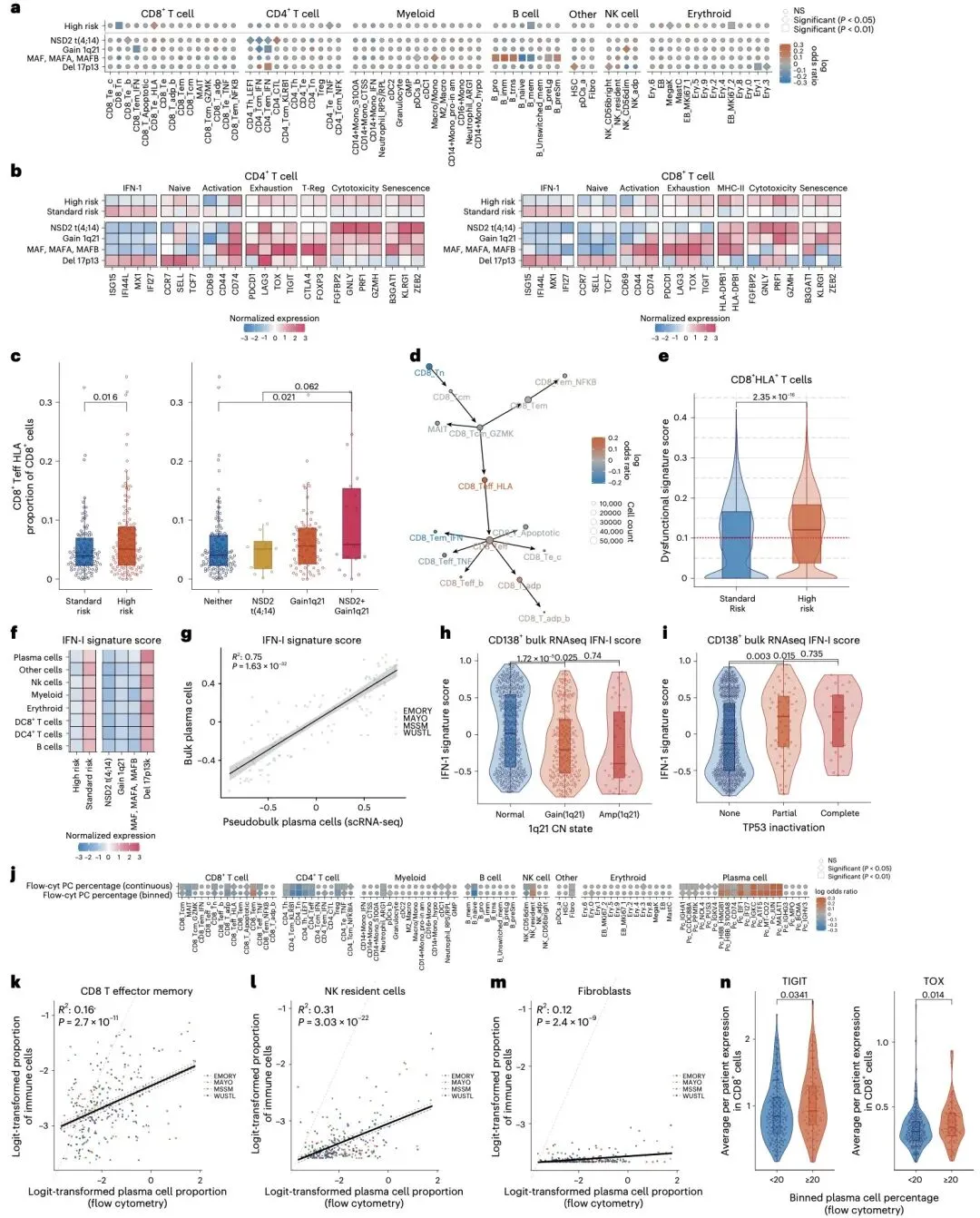
疾病进展相关分析揭示了快速进展者的核心免疫特征:与持续缓解 4 年以上的患者相比,18 个月内疾病进展的患者骨髓中 CD4+ T 细胞和 B 细胞数量减少,髓系细胞和浆细胞比例升高,且存在促炎免疫衰老相关分泌表型。快速进展者的 CD8+ T 细胞呈现终末分化特征,初始 T 细胞池枯竭,同时伴随 TIGIT、TOX 等耗竭标志物表达升高,提示免疫功能衰竭是疾病进展的重要驱动因素。
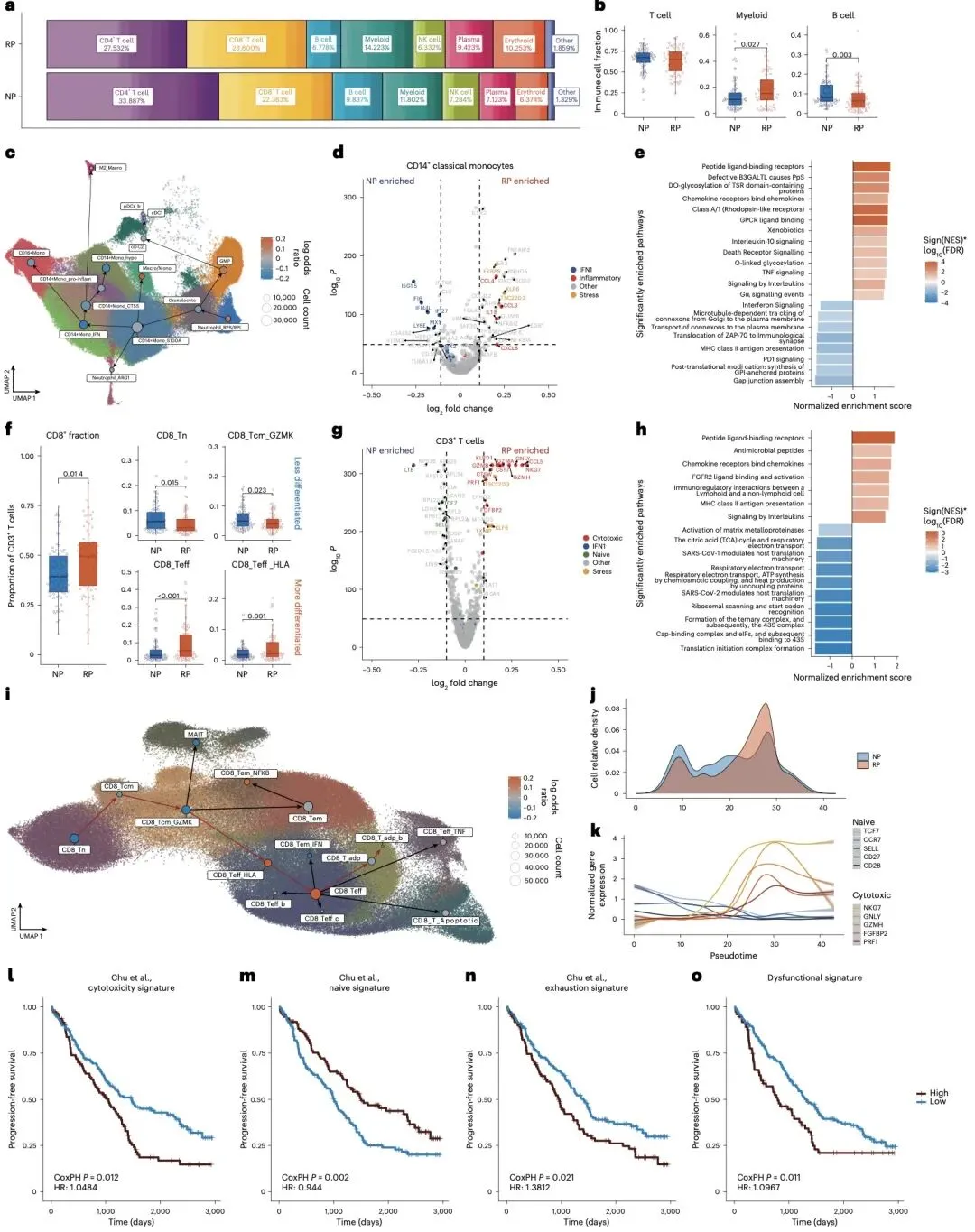
细胞间通讯分析发现,增殖诱导配体(APRIL)和 B 细胞成熟抗原(BCMA)介导的信号通路在肿瘤微环境中异常活跃,可能促进肿瘤细胞存活。此外,快速进展者的髓系细胞高表达 IFNγ 受体,而 IFNγ 信号通路的过度激活与不良预后相关,成为潜在治疗靶点。
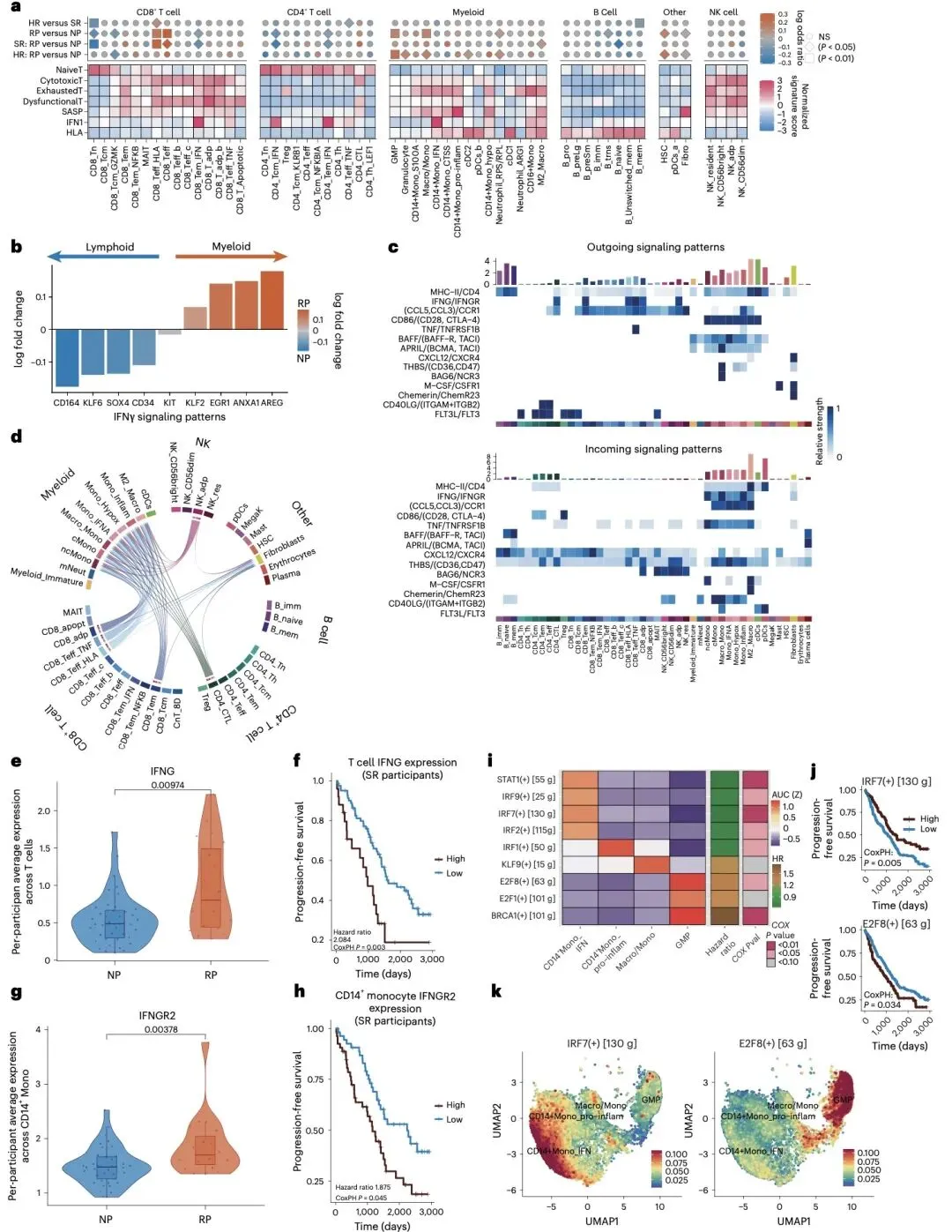
研究的核心突破在于建立了整合免疫特征、细胞遗传学和临床指标的预后预测模型。该模型在验证队列中表现出优异性能,预测无进展生存期的 AUC 值高达 0.94,显著优于传统临床指标联合细胞遗传学的预测模型(AUC=0.73)。其中 11 个关键免疫亚群(包括 CD8 + 效应 T 细胞、炎症性髓系细胞等)构成的最小签名集,为开发简化的临床检测方法奠定了基础。
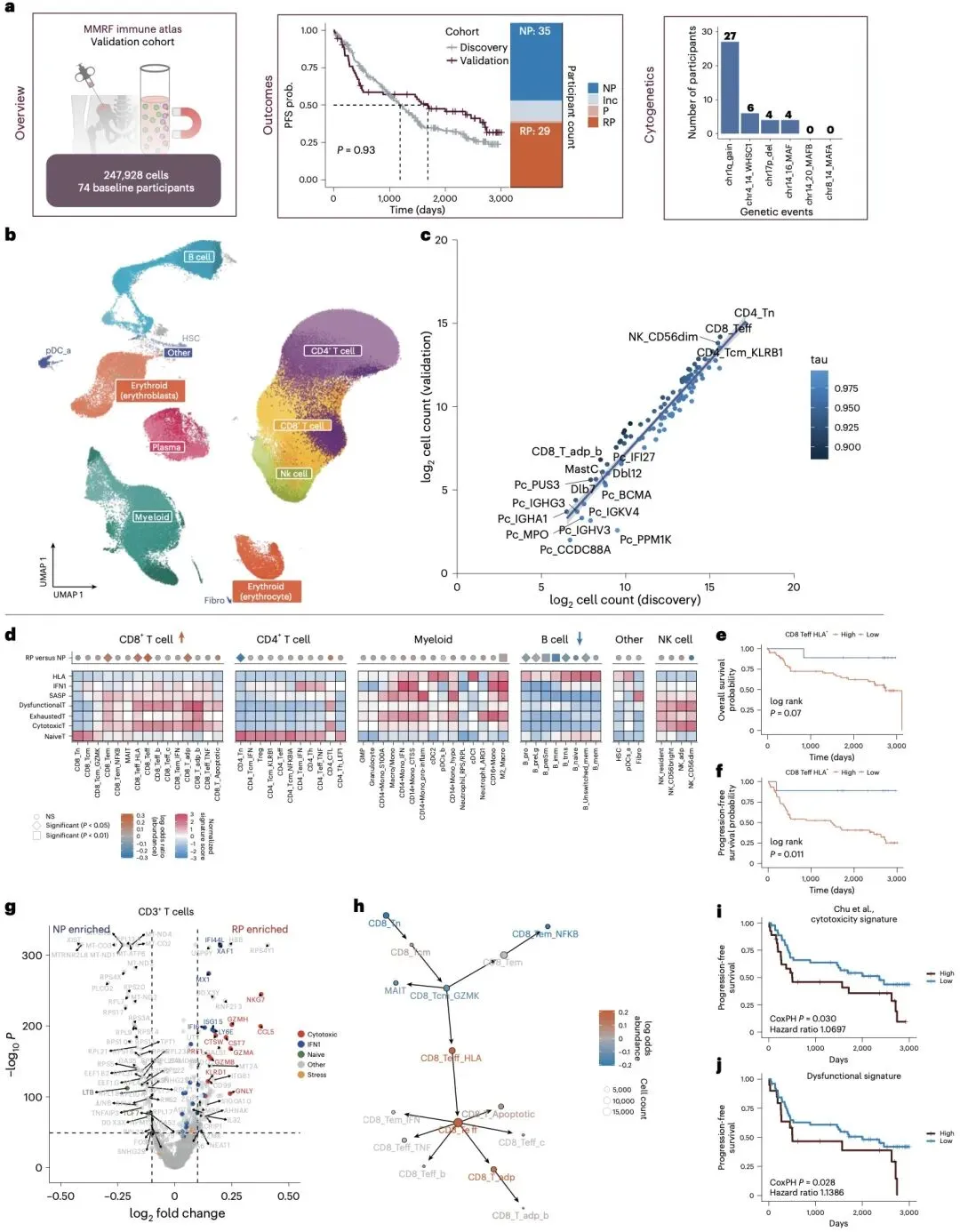
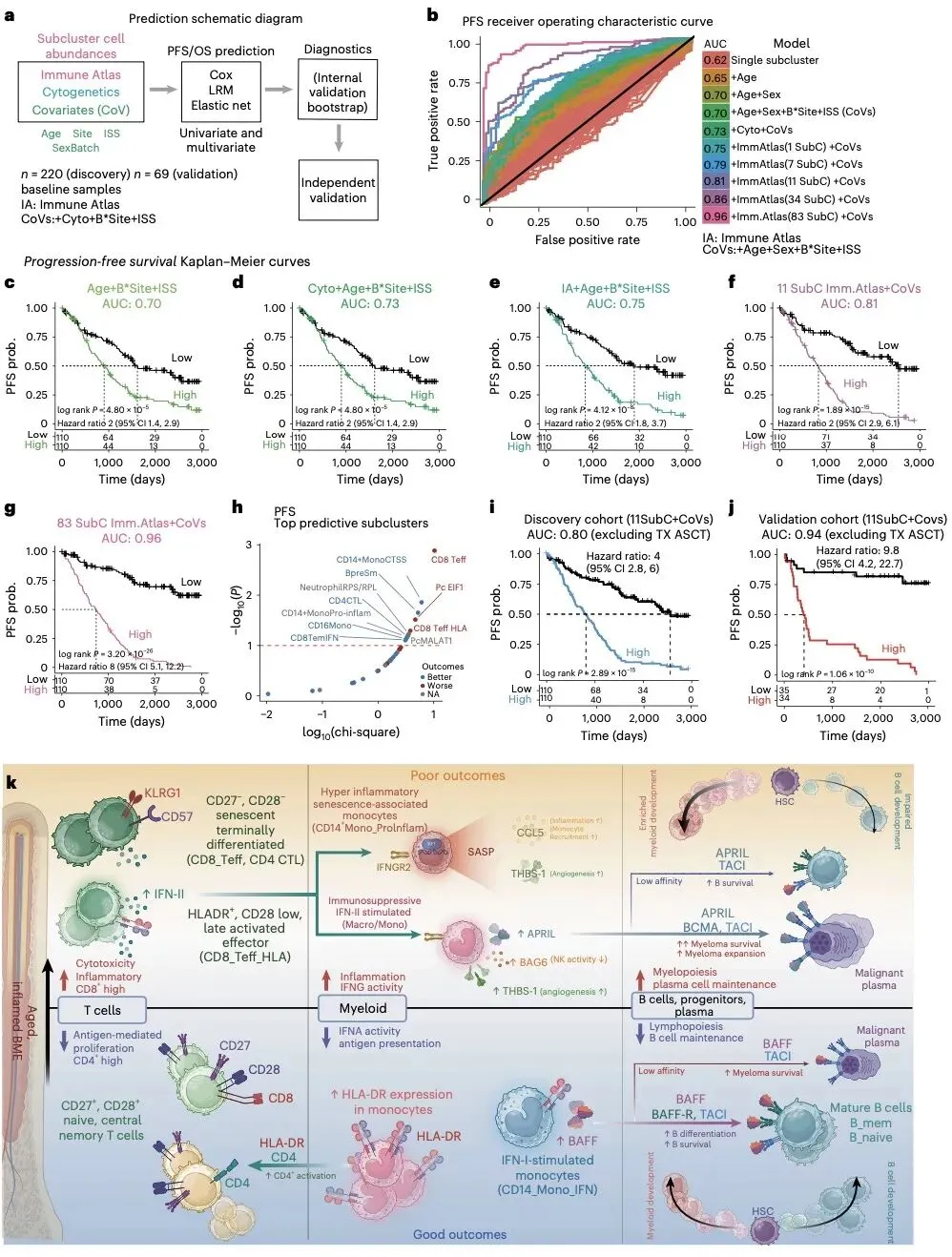
该免疫图谱揭示了骨髓免疫微环境在多发性骨髓瘤中的关键作用,即使在遗传背景良好的患者中,免疫衰老和炎症微环境也可能导致不良结局。
(我们自己开发的服务器,很多意想不到的功能
免💰服务器地址:https://vip.r-py.com/)
生信钱同学团队提供生信便捷式“云服务器”、“数据分析”、“生信学习班”以及“生信交流群”等内容,有需要者可以加我:sx_qtx01
相关推文内容:
今天开课了,没服务器直接送——多组学与机器学习联合分析(机器学习分析代谢组、蛋白组、宏基因组、网络药理学、转录组课)
学生信当然要与时俱进了,零基础也能学的AI生信课(AI助力生信入门班即将开始(AI课)
超多生信内容学习,感兴趣可以了解下(单细胞课程)
没有服务器,单细胞数据搞不定?看看我们做出来的结果包含啥?我们目前做好了这些pipeline,可以帮你做(数据分析) 公共共享服务器已开启,无门槛尽管用,不限制资源(免💰服务器) 今晚 7 点开始,12节线上课,不收费,把开源的QuPath病理和荧光图像分析的技巧学明白 手把手复现Nature的生信教学即将开始,感兴趣的可以了解下 当我同学用这个套路发了10几篇SCI,并拿了国奖,我惊呆了——文献计量学+AI大语言模型学习(文献计量培训) Gemini详细安装教程,自动分析数据,不是器械式写代码,而是帮你做好,就是这么智能(AI自动写代码,自动分析数据)